Recherche & douleurs oculaires - Partie 2

PARTIE 2
La surface oculaire est le siège de nombreuses pathologies à l’origine de douleurs oculaires. Il faut savoir que l’innervation nociceptive se situe essentiellement sur le segment antérieur de l’œil, comprenant la cornée, la conjonctive, l’iris et les corps ciliaires, quand le segment postérieur (rétine) est quant à lui peu innervé. Il n'y a rien d'étonnant à ce que la moindre agression de la cornée ou une lésion des nerfs cornéens provoquent une douleur d’une très forte intensité : la cornée est en effet le plus puissant générateur de douleur de tout l’organisme puisqu’elle est le tissu le plus densément innervé du corps. On estime à 7000/mm2 la densité des terminaisons nerveuses cornéennes chez l’homme. Par comparaison, cette densité est 500 fois plus élevée que celle du derme et 30 fois plus que la pulpe dentaire. On comprend ainsi que toute altération, stimulation ou abrasion de la cornée peut conduire à une douleur particulièrement forte.
Vers le développement de nouvelles cibles thérapeutiques
Depuis deux ans, l'équipe de l'Institut de la Vision a publié plusieurs articles portant sur l’identification et la validation de cibles bien spécifiques présentes sur les terminaisons nerveuses de la cornée. Pour rappel, la cornée est le tissu le plus innervé de l'organisme et cette innervation est composée de différents types de récepteurs sensoriels exprimés sur les fibres nerveuses. Parmi eux, les nocicepteurs polymodaux sont capables de répondre à plusieurs stimulations, qu'elles soient de nature mécanique, thermique ou chimique. Ces fibres expriment des marqueurs à l'instar du marqueur TRPV1, un canal ionique sensible à la capsaïcine qui, lorsqu'il est activé, est capable d’induire une douleur. En aparté, le prix Nobel de médecine 2021 a mis les neurosciences à l’honneur en récompensant les neurophysiologistes américains David Julius et Ardem Patapoutian. En identifiant d'abord le récepteur TRPV1 puis d'autres capteurs, ils ont découvert par quels mécanismes étaient déclenchées les impulsions nerveuses permettant de percevoir les variations de température et de pression provenant de notre environnement. “Nos récentes études ont montré qu’un blocage pharmacologique de certaines cibles (TRPV1 ou TRPM8), au travers de traitements topiques chez les animaux - traités de façon bi quotidienne sur plusieurs jours, pour mimer les traitements topiques chez le patient -, est capable de bloquer l'hypersensibilité cornéenne mais également tous les mécanismes neuro-inflammatoires périphériques ou centraux associés à ces douleurs cornéennes”, poursuit le Dr Réaux-Le Goazigo. Une découverte de taille donc pour l'équipe de l'Institut de la Vision qui a su montrer en recherche fondamentale qu’une douleur oculaire avait donc un impact au niveau du système nerveux central.
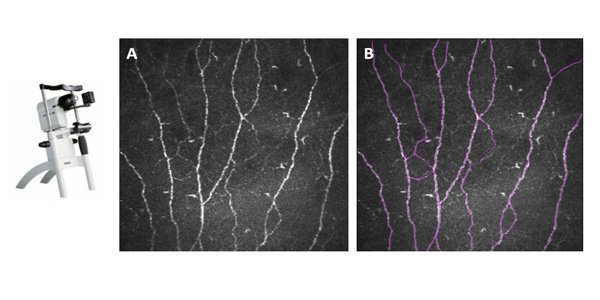
En photo : Microscopie Confocale In Vivo // A) Nerfs Cornéens // B) Traçage des nerfs à l'aide d'un logiciel ImageJ pour quantifier leur densité
De la recherche fondamentale à la recherche clinique
Les recherches à l’Institut de la Vision sont particulièrement complémentaires avec toute la recherche clinique réalisée au CHNO des Quinze-Vingts. L'établissement a d'ailleurs mis en place la première et unique unité de consultation dédiée à la douleur oculaire (UDO), sous l'impulsion et la direction du Pr Christophe Baudouin. Ainsi, en recherche clinique, une collaboration est par exemple menée avec le service de neuro-imagerie du Dr Christophe Habas : une étude est actuellement en cours pour mieux comprendre grâce à l'IRM fonctionnel les changements morphologiques et fonctionnels qui se produisent dans le cerveau des patients souffrant de douleurs oculaires. “Nous commençons à mieux comprendre les mécanismes et les voies nerveuses mises en jeu dans la douleur oculaire dans nos modèles animaux. Il est désormais important d’identifier plus précisément les structures cérébrales qui vont être activées ou désactivées dans ce contexte de douleur oculaire chronique chez le patient”, ajoute la neurobiologiste. Notamment chez des patients qui souffrent de douleurs oculaires et qui s'avèrent réfractaires à tous les traitements et thérapies combinatoires actuelles. “Au travers de questionnaires bien spécifiques et une exploration de la surface oculaire, nous avons les moyens d'identifier si ces patients souffrent de douleurs oculaires neuropathiques.”
Vers des traitements personnalisés
La sécheresse oculaire est une pathologie très complexe qui peut mener à des douleurs chroniques en raison soit d'une mauvaise production de larmes (sécheresse dite aqueuse), soit d'une mauvaise qualité des larmes (sécheresse dite évaporative). Les équipes de recherche ont ainsi pu observer qu'en fonction de l’étiologie, c'est-à-dire la forme aqueuse ou évaporative de la sécheresse oculaire, les altérations morphologiques des nerfs cornéens différaient. “Nos travaux visent à mieux caractériser ces atteintes nerveuses dans les différentes cohortes de patients douloureux avec l'idée, dans un futur proche, d’être en mesure de leur proposer un traitement personnalisé. In fine, l’utilisation de questionnaires spécifiques, les examens cliniques réalisés lors de la consultation dédiée à la douleur oculaire et l'imagerie des nerfs cornéens, nous aident à mieux comprendre la douleur oculaire dont souffrent les patients (qu’elle soit d’origine inflammatoire ou neuropathique)”, indique la chercheuse Inserm. Autre point très important de la recherche : la quête de biomarqueurs permettant de caractériser la douleur et d'aiguiller vers de nouvelles pistes thérapeutiques. “Pour identifier et évaluer certains biomarqueurs ou molécules d'intérêt, nous avons la possibilité d'analyser le contenu cellulaire d’empreintes conjonctivales réalisées chez les patients, et nos travaux ont permis de détecter des marqueurs pro-inflammatoires, et des molécules déjà connues dans le monde de la douleur. Mais l'idée est de savoir maintenant si ces molécules sont surexprimées dans les différentes cohortes de patients et, éventuellement, si ces marqueurs candidats peuvent être régulés (diminués) lorsqu'un traitement antalgique est mis en place”, conclut Le Dr Annabelle Réaux-Le Goazigo. La recherche se poursuit donc bel et bien : après avoir mis en évidence les changements cellulaires et moléculaires tout au long de la voie nociceptive, les études actuellement en cours à l'Institut de la Vision devraient permettre de mieux comprendre les changements plastiques qui s’opèrent dans le cerveau des patients. À terme, pour offrir de nouvelles perspectives dans la découverte de mécanismes et médicaments innovants permettant de soulager les patients.
L'éventail thérapeutique est à ce jour très limité chez les patients souffrant de douleurs oculaires chroniques, allant de collyres immunomodulateurs aux traitements médicamenteux “classiques” des douleurs neuropathiques (antidépresseurs tricycliques, antiépileptiques...). Néanmoins, de nombreux patients résistent à ces traitements, d'où l'idée de trouver de nouvelles pistes thérapeutiques, mais aussi d'améliorer les traitements par voie topique car les nerfs cornéens sont directement accessibles par l'intermédiaire de l'instillation de gouttes dans l'œil.

En photo : Dr Annabelle Réaux-Le Goazigo, du centre de recherche de l'Institut de la Vision, INSERM / CNRS / Sorbonne Université. © Institut de la Vision - SU/LArdhuin
Photo en tête d'article © Institut de la Vision - SU/LArdhuin
À lire aussi

Douleur oculaire, mieux comprendre ses mécanismes pour mieux la traiter à l'Institut de la Vision
PARTIE 1
Douleur oculaire, une prise en charge unique au CHNO des Quinze-Vingts
La sécheresse oculaire est l’un des premiers motifs de consultation dans les cabinets d’ophtalmologie&nbs

Le Guide de la Vue, édition mars 2022
Le Guide de la Vue Le mag N°33 vient de sortir !








